我院翁群红课题组近日在Wiley综合性期刊Advanced Science上(IF=15.84)以Biodegradable and Peroxidase-Mimetic Boron Oxynitride Nanozyme for Breast Cancer Therapy (DOI:10.1002/advs.202101184)为题报道了一种具有类似过氧化物酶功能的氮化硼纳米药物,可高效催化癌细胞内源性过氧化氢生成羟基自由基,对乳腺癌具有显著的抑制和治疗作用。这是氮化硼继硼中子俘获治疗(BNCT)、活性硼疗法和药物递送后发现的又一抗肿瘤新进展。
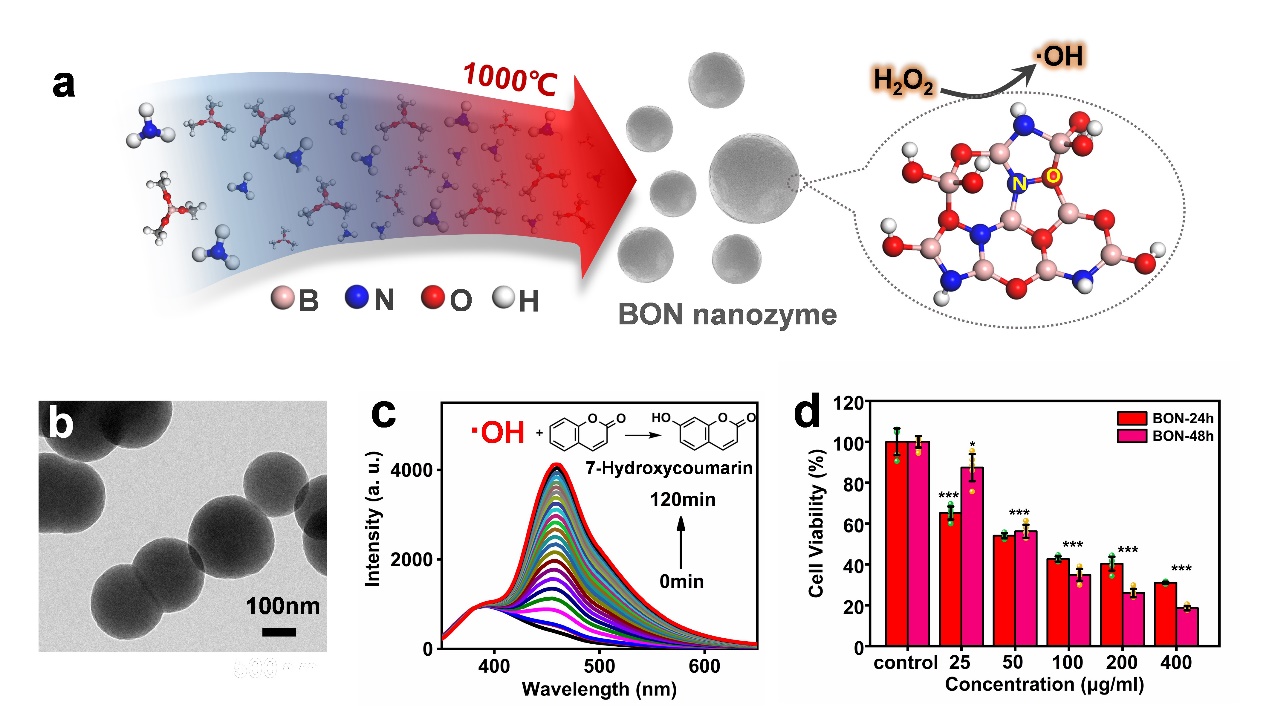
图1. (a)高温裂解合成BON纳米酶示意图;(b)透射电镜图;(c)体外催化生成羟基自由基实验;(d)4T1细胞抑制实验。
六方氮化硼(h-BN)具有类似石墨的结构,拥有优异的化学稳定性和热稳定性,是一种生物相容性极好的材料,已被广泛添加到高端化妆品中,在生物医药方面也显示出巨大的应用潜力。氮化硼由于其独特的性质,经功能化后可作为纳米药物在肿瘤诊断和治疗方面发挥独特而重要的作用。
翁群红课题组在研究活性硼疗法过程中,发现了一种经高温裂解得到的氮化硼功能材料富含N-O键,不仅能在体外高效催化过氧化氢分解生成羟基自由基,而且还可经细胞内吞富集于溶酶体中,原位催化4T1乳腺癌细胞中内源性过氧化氢分解生成具有高细胞毒性的羟基自由基,诱导癌细胞凋亡。经氮化硼纳米酶48小时的作用,癌细胞的存活率降低了82%。小鼠实验表明,该氮化硼纳米酶对乳腺肿瘤有强烈的抑制作用,经14天的对比治疗后,发现其生长抑制率与对照组相比为97%,治疗效果分别为惰性氮化硼纳米材料的10倍、活性硼疗法的1.3倍。该氮化硼纳米酶本身在水溶液中经7天可被降解。
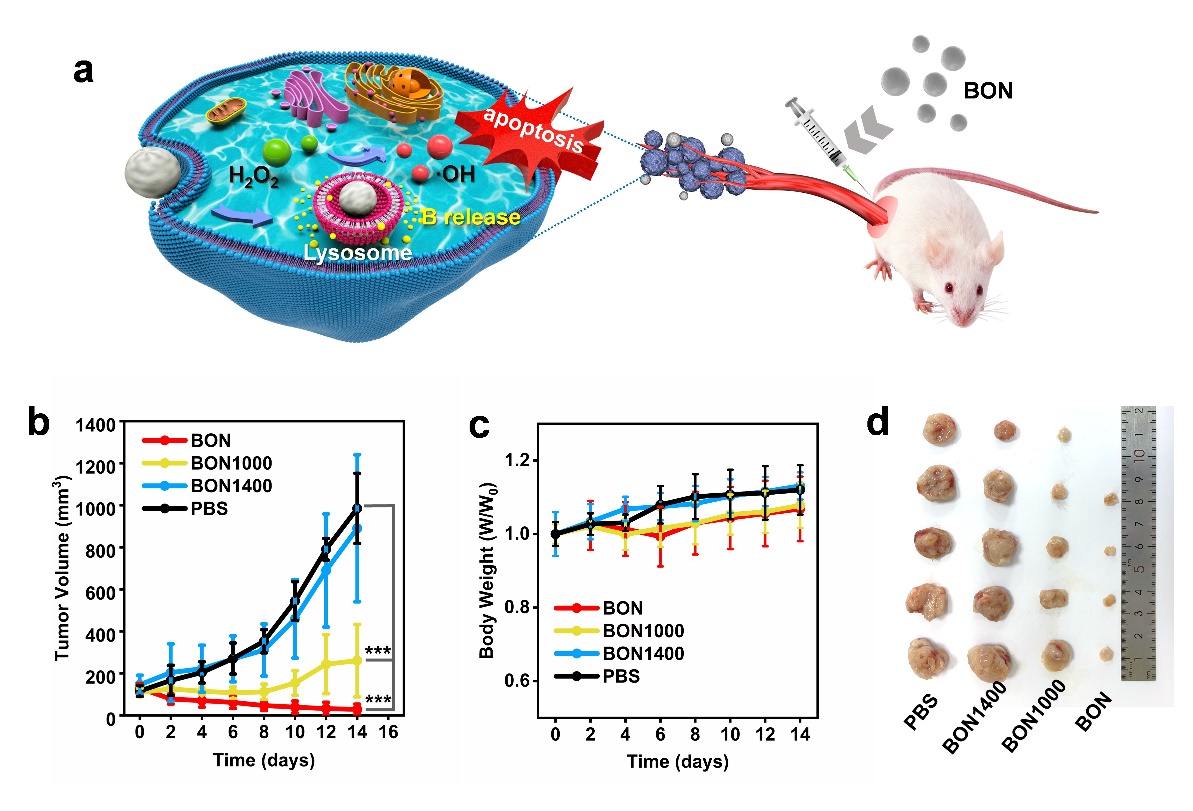
图2. (a) BON纳米酶抗癌作用示意图;(b)小鼠肿瘤抑制实验;(c)小鼠体重变化;(d)经14天治疗后肿瘤组织对比。
该工作发现并证明了氮化硼通过纳米酶作用抗肿瘤的机制,为发展集成多种癌症诊断和治疗功能于一体的氮化硼纳米诊疗平台提供了新的工具和途径。第一作者为硕士生曾璐拉,研究得到了陈美副教授和葛行义教授在动物实验技术上的支持,以及国家自然科学基金和湖湘高层次人才聚集工程的资助。工作被Wiley Advanced Science News报道。
翁群红教授自2018年加入湖南大学材料学院建立课题组,围绕氮化硼生物医用材料、微储能器件&系统开展了深入研究,以湖南大学为第一单位的研究进展陆续发表在Adv. Sci., Adv. Funct. Mater.,Small,ChemSusChem,Mater. Adv., Ceram. Int.等专业期刊,多项工作被Wiley的Materials Views China, Advanced Science News, X-MOL等媒体报道:
https://www.materialsviewschina.com/2021/03/52934/;
https://www.materialsviewschina.com/2020/10/49902/;
https://www.x-mol.com/news/676715。

